Dlí Hess
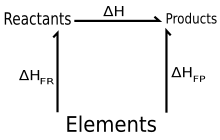
Sonraíonn Dlí Hess go bhfuil an t-athrú eantalpachta d’imoibriúcháin neamhspleách ar an bhealach a leantar, chomh fada is go bhfuil na dálaí tosaigh agus deiridh mar an gcéanna.
Ainmnítear an dlí i ndiaidh Germain Hess, ceimiceoir agus lia Rúiseach a rugadh san Eilvéis a d’fhoilsigh é i 1840.
Tuigtear anois dlí Hess mar léiriú ar phrionsabal imchoimeád an fhuinnimh, arna chur in iúl freisin i gcéad dlí na teirmidinimice, prionsabal a shonraíonn nach féidir fuinneamh a chruthú ná a scrios, ach is féidir é a athrú ó fhoirm amháin go foirm eile.[1][2] Is féidir athruithe imoibrithe eantalpachta a chinneadh trí chalraiméadracht do go leor imoibrithe. De ghnáth luaitear na luachanna do phróisis a bhfuil na teochtaí agus na brúnna tosaigh agus deiridh céanna acu, cé gur féidir leis na dálaí athrú le linn an imoibrithe. Is féidir dlí Hess a úsáid chun an fuinneamh foriomlán a theastaíonn le haghaidh imoibrithe cheimicigh a chinneadh, nuair is féidir é a roinnt ina chéimeanna sintéiseacha atá níos éasca a thréithriú ina n-aonar. Tugann sé seo tiomsú eantalpachtaí caighdeánacha déanmhaíochta, a fhéadfar a úsáid mar bhunús chun sintéisí casta a dhearadh.
Teoiric
cuir in eagarDeirtear i ndlí Hess go bhfuil athrú na heantalpachta in imoibriú ceimiceach (i.e. teas imoibriúcháin ag brúthairiseach) neamhspleách ar an gconair idir an staid tosaigh agus na staideanna deireanacha.
Tuilleadh léitheoireachta
cuir in eagar- Leicester, Henry M. (1951). "Germain Henri Hess and the Foundations of Thermochemistry". The Journal of Chemical Education 28 (11): 581–583. doi:. Bibcode: 1951JChEd..28..581L.
Naisc sheachtracha
cuir in eagar- COMHAD FÍRICÍ:CEIMIC GCE.https://ccea.org.uk/downloads/docs/Support/Comhad%20F%C3%ADric%C3%AD%3A%20AS/2019/Comhad%20F%C3%ADric%C3%AD%3A%202.8%3A%20Fuinneamhachas.pdf
- Hess' paper (1840) on which his law is based (at ChemTeam site)
- http://www.adamequipment.com/education/Documents/experiment_6.pdf Curtha i gcartlann 2016-03-03 ar an Wayback Machine a Hess’ Law experiment
Tagairtí
cuir in eagar- ↑ Dlí Hess faoi Theas-Suimiúchán. Ó Cinnéide, Ceimic Bhunúsach 1, Oifig an tSoláthair 1975.
- ↑ Hess's Law The principle of conservation of energy. https://web.archive.org/web/20150109195637/http://www.science.uwaterloo.ca/~cchieh/cact/c120/hess.html